酸化銅の還元の中学生向け解説ページです。
「酸化銅の還元」
は中学2年生の化学で学習します。
- 還元とは何か
- 酸化銅の還元の実験動画
- 酸化銅の還元の化学反応式(炭素)
- 酸化銅の還元の化学反応式(水素)
を学習したい人は
このページを読めばバッチリだよ!
中学理科の成績を伸ばせる塾!「さわにい理科塾」を始めました!詳しく知りたい方はこちら。さわにい本人のサポートで成績UPです!
では、酸化銅の還元の学習スタート!
(目次から好きなところに飛べるよ)
還元とは
還元とは、
物質から酸素が取り除かれる化学反応
のことだよ!
 ねこ吉
ねこ吉物質から酸素が取り除かれる化学反応?
うん。
このページで紹介する「酸化銅 ![]()
![]()
「銅原子 ![]()
![]()
![]()
![]()
が化合して(くっついて)できたものだね。
最新の学習指導要領では「化合」を「物質と結びつく化学変化」と表現します。
この酸化銅のように、酸素がくっついたものから、酸素原子を取り除く化学変化を
「還元」
というんだよ!



酸化銅から酸素を取り除くなんて出来るの?
簡単にできるよ☆
酸素ちゃん(![]()
![]()
銅君(![]()
![]()
酸化銅(![]()
![]()
イケメンの炭素君(![]()
![]()
簡単に銅から酸素を引き離せるんだ☆
なんて例えだ…。
図で表すと…


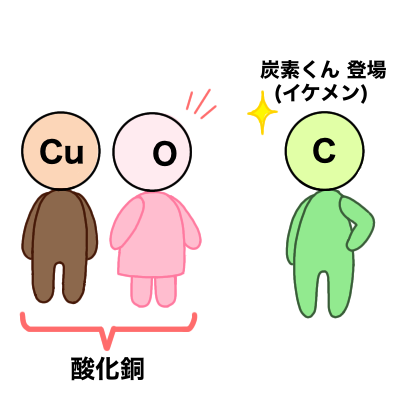



銅と酸素が分かれて還元完了だね☆



悲しい話や…。
酸化銅の還元の実験
では、酸化銅の還元の実験を見てみよう。
「酸化銅」は黒色の物質だね!


これを還元して銅にもどすよ!



炭素を連れてくるんだね。
うん。下の写真が炭素だよ。


酸化銅と炭素を混ぜて、かき混ぜるよ!


この時点では、まだ還元は起きていないよ!



どうすれば還元が起きるの?
この、酸化銅と炭素の混合物を加熱すればいいんだ。
では、さっそく実験動画を見てみよう!
ポイントは2つ!
- 酸化銅は酸素と分かれ、銅になる。
- 炭素は酸素とくっつき、二酸化炭素になる
の2点だよ!



おー。めっちゃ反応してる!
ほんとだね!
これにより、「酸化銅」は「銅」になったよ!


銅の「赤褐色」になっているね。



10円玉の色だね。
うん。裏から見ると、もっとよく分かるよ!





ほんとだ!酸化銅→銅になったんだね!
ところで、
銅と離れた「酸素」はどこにいったか分かるかな?



「炭素」とくっついたんでしょ?
その通り。酸素は銅と離れ、炭素とくっついたんだ!
では、炭素と酸素がくっつくと、何になるかな?



えーと、何だろう?
この実験では、炭素と酸素がくっついて、二酸化炭素になったんだよ!
実験動画で「石灰水」が白く濁っているね!
これは二酸化炭素が発生した証拠なんだ!
しっかりと、覚えておこうね!



はーい!
酸化銅の還元の化学反応式
最後に銅の酸化(燃焼)の化学反応式を確認しよう!
酸化銅の還元で使う化学式
まずは化学式の確認だよ。
酸化銅の化学式は
CuO だね。
モデル(絵)で書くと


だね。
炭素の化学式は
C だね。
モデル(絵)で書くと


だね。
次に、
銅の化学式は
Cu だね。
モデル(絵)で書くと


だね。
最後に、
二酸化炭素の化学式は
CO2 だね。
モデル(絵)で書くと


だね。
まずはこの化学式をしっかりと覚えてね!



化学式を正確に覚えないと、化学反応式は書けないんだよね!
そうそう。特に、
「酸化銅」は銅と酸素が1つずつ
というところをしっかりと覚えようね!
炭素を使った酸化銅の還元の化学反応式
では、炭素を使った
酸化銅の還元の化学反応式を確認しよう。
酸化銅の還元の化学反応式は下のとおりだよ!
2CuO + C → 2Cu + CO2
だよ!



先生、式の書き方はどうだっけ?
では、1から解説するね。
まず、日本語で化学反応式を書いてみよう!
① 酸化銅 + 炭素 → 銅 + 二酸化炭素
(慣れたら省略していいよ。)
次に、①の日本語を化学式にそれぞれ変えるよ。
② CuO + C → Cu + CO2
だね。
これで完成にしたいけれど、
CuO + C → Cu + CO2
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
このままでは、矢印の左と右で原子の数が合っていないね。



矢印の左側に酸素原子が1つ足りないね。
うん。
この場合は両側で原子の数を合わせないといけないんだよ。
それでは係数をつけて、原子の個数を矢印の左右でそろえていくよ。
係数は化学式の前、
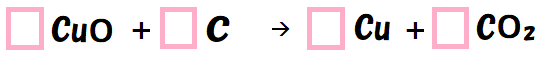
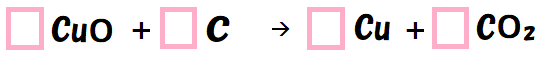
のピンクの四角の中にしか書いてはいけないね。
右下の小さい数字を書いたり変えたりしないでね。
それでは係数を書いて、左右の原子の個数をそろえよう。
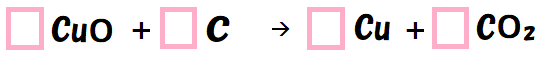
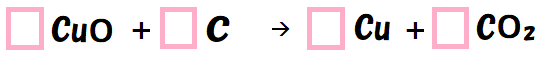
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
今、矢印の左側の酸素原子が1個たりないね。
足りない所を増やしていけば、いつか必ず数がそろうよ。
では、左側の酸化銅の前に係数をつけて、増やしてみよう。


![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
これで左右の酸素原子の数がそろったね!



だけど、銅原子の数が合わなくなってしまったよ!
うん。では、今度は矢印の右側に銅を増やそう。
足りない所を増やしていけば、いつか必ず数がそろうからね。


![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
これで、矢印の左右で原子の数がそろったね。
つまり、化学反応式の完成なんだね。
炭素による酸化銅の還元の化学反応式は
2CuO + C → 2Cu + CO2
だね!
水素を使った酸化銅の還元の化学反応式
これで解説は終わりなんだけど、
酸化銅は、炭素の代わりに水素を使っても還元ができるんだ。
その場合の化学反応式も解説して終わりにするよ!
水素を使った酸化銅の還元の化学反応式は下のとおりだよ!
CuO + H2 → Cu + H2O
だよ!
水素を使うと、還元後に水ができると覚えておこう。
それさえ覚えておけば、後は簡単だよ!
では化学反応式の書き方を1から確認しよう。
まず、日本語で化学反応式を書いてみよう!
① 酸化銅 + 水素 → 銅 + 水
(慣れたら省略していいよ。)
次に、①の日本語を化学式にそれぞれ変えるよ。
② CuO + H2 → Cu + H2O
だね。
矢印の左と右の原子の数を確認しよう。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
- 銅原子が1つ
- 水素原子が2つ
- 酸素原子が1つ
と、矢印の左右で原子の数がそろっているね。
この場合は「係数」という大きい数字をつけて数合わせをしないでいいね!
だから、これで化学反応式は完成なんだ!
水素による酸化銅の還元の化学反応式は
CuO + H2 → Cu + H2O
だね!
化学反応式が苦手な人は、下のボタンから学習してみてね!
他の中学2年実験解説は下のリンクを使ってね!
実験動画つきでしっかり学習できるよ!



またねー
さわにいは、登録者8万人の教育YouTuberです。
中学の成績を上げたい人は、ぜひYouTubeも見てみてね!
また、2022年10月に学習参考書も出版しました。よろしくお願いします。
他のページも見たい人はトップページへどうぞ。


今なら相談無料です












コメント
コメント一覧 (2件)
めっちゃ分かりやすいです!
ありがとうございます!
お役に立ててよかったです!